Содержание
- 1 Что такое Уран
- 2 Открытие.
- 3 Месторождения урановых руд в России
- 4 Крупнейшие месторождения по добыче урана в мире – страны лидеры
- 5 Запасы и объемы добычи урановой руды в России
- 6 Минералы, руды, добыча
- 7 Свойства Урана
- 8 Характеристики урана
- 9 Кристаллические формы
- 10 Уран в мире
- 11 Уран и ядерные бомбы
- 12 Получение
- 13 Сплавы, соединения
- 14 Уран и производство электричества
- 15 Плюсы и минусы
Что такое Уран
Уран — это радиоактивный химический элемент, который можно найти в природе. В основном он используется для производства электрической энергии. Впрочем, его также используют в медицинских целях и, к сожалению, при производстве ядерных бомб.
Этот элемент был открыт на территории Германской империи в 1789 году. Он назван в честь планеты Уран, которая была обнаружена на 8 лет раньше. Однако радиоактивность урана была открыта лишь в 1896 году.
Уран — последний элемент в таблице Менделеева. Он ещё и самый тяжёлый элемент, существующий в естественном виде на Земле. Именно при расщеплении его атома получается электричество.
Электричество, которое производится из урана, является альтернативой горючим ископаемым, таким как нефть и уголь. Сегодня 16% электричества в мире получается из урана.

Урановая руда
Открытие.
Уран был открыт в 1789 немецким химиком М.Клапротом, который присвоил имя элементу в честь открытия за 8 лет перед этим планеты Уран. (Клапрот был ведущим химиком своего времени; он открыл также другие элементы, в том числе Ce, Ti и Zr.) В действительности вещество, полученное Клапротом, было не элементным ураном, но окисленной формой его, а элементный уран был впервые получен французским химиком Э.Пелиго в 1841. С момента открытия и до 20 в. уран не имел того значения, какое он имеет сейчас, хотя многие его физические свойства, а также атомная масса и плотность были определены. В 1896 А.Беккерель установил, что соли урана обладают излучением, которое засвечивает фотопластинку в темноте. Это открытие активизировало химиков к исследованиям в области радиоактивности и в 1898 французские физики супруги П.Кюри и М.Склодовская-Кюри выделили соли радиоактивных элементов полония и радия, а Э.Резерфорд, Ф.Содди, К.Фаянс и другие ученые разработали теорию радиоактивного распада, что заложило основы современной ядерной химии и атомной энергетики.
Радиоактивность
Создание периодической системы российским химиком Дмитрием Менделеевым в 1869 году сосредоточило внимание на уране как на самом тяжелом из известных элементов, которым он оставался до открытия нептуния в 1940 г. В 1896-м французский физик Анри Беккерель обнаружил в нем явление радиоактивности. Это свойство позже было найдено во многих других веществах. Теперь известно, что радиоактивный во всех его изотопах уран состоит из смеси 238U (99,27 %, период полураспада — 4 510 000 000 лет), 235U (0,72 %, период полураспада — 713 000 000 лет) и 234U (0,006 %, период полураспада — 247 000 лет). Это позволяет, например, определять возраст горных пород и минералов для изучения геологических процессов и возраста Земли. Для этого в них измеряется количество свинца, который является конечным продуктом радиоактивного распада урана. При этом 238U является исходным элементом, а 234U – один из продуктов. 235U порождает ряд распада актиния.
Открытие цепной реакции
Химический элемент уран стал предметом широкого интереса и интенсивного изучения после того, как немецкие химики Отто Хан и Фриц Штрассман в конце 1938 г. при его бомбардировке медленными нейтронами обнаружили в нем ядерное деление. В начале 1939 г. американский физик итальянского происхождения Энрико Ферми предположил, что среди продуктов расщепления атома могут быть элементарные частицы, способные породить цепную реакцию. В 1939 г. американские физики Лео Сциллард и Герберт Андерсон, а также французский химик Фредерик Жолио-Кюри и их коллеги подтвердили это предсказание. Последующие исследования показали, что в среднем при делении атома высвобождается 2,5 нейтрона. Эти открытия привели к первой самоподдерживающейся цепной ядерной реакции (02.12.1942), первой атомной бомбе (16.07.1945), первому ее использованию в ходе военных действий (06.08.1945), первой атомной подводной лодке (1955) и первой полномасштабной атомной электростанции (1957).

Состояния окисления
Химический элемент уран, являясь сильным электроположительным металлом, реагирует с водой. Он растворяется в кислотах, но не в щелочах. Важными состояниями окисления являются +4 (как в оксиде UO2, тетрагалогенидах, таких как UCl4, и зеленом водном ионе U4+) и +6 (как в оксиде UO3, гексафториде UF6 и ионе уранила UO22+). В водном растворе уран наиболее устойчив в составе иона уранила, обладающего линейной структурой [О = U = О]2+. Элемент также имеет состояния +3 и +5, но они неустойчивы. Красный U3+ медленно окисляется в воде, которая не содержит кислорода. Цвет иона UO2+ неизвестен, поскольку он претерпевает диспропорционирование (UO2+ одновременно сводится к U4+ и окисляется до UO22+) даже в очень разбавленных растворах.
Месторождения урановых руд в России
Россия считается одним из мировых лидеров по добыче урановых руд. На протяжении последних нескольких десятков лет Россия стабильно входит в топ-7 стран-лидеров по этому показателю.
Наиболее крупными месторождениями этих природных минеральных образований являются:
| Месторождение | Область | Запасы чистого урана, тонн | Комментарий |
| Аргунское | Читинская область | 9481 | Самое крупное российское месторождение. Дает 93% от общего объема добычи. |
| Жерловое | Читинская область | 3485 | Общие запасы оценивают в 4137 тысяч тонн. |
| Хиагдинское | Бурятия | 11300 | Разработка месторождений проходит методом подземного выщелачивания. Хиагдинское поле состоит из 8 месторождений. |
Крупнейшие месторождения по добыче урана в мире – страны лидеры
Добыча урановой руды в шахте
Мировым лидером по добыче урана считается Австралия. В этом государстве сконцентрировано более 30% всех мировых запасов. Наиболее крупными австралийскими месторождениями являются Олимпик Дам, Биверли, Рейнджер и Хонемун.
Что такое руда? Какие виды руды бывают? Как её добывают? Страны-лидеры по добыче руды
Главным конкурентом Австралии считается Казахстан, на территории которого содержится практически 12% мировых запасов топлива. На территории Канады и ЮАР сконцентрировано по 11% мировых запасов урана, в Намибия – 8%, Бразилии – 7%. Россия замыкает семерку лидеров с 5%. В список лидеров также входят такие страны, как Намибия, Украина и Китай.
Крупнейшими мировыми урановыми месторождениями являются:
| Месторождение | Страна | Начало обработки |
| Олимпик-Дэм | Австралия | 1988 |
| Россинг | Намибия | 1976 |
| МакАртур-Ривер | Канада | 1999 |
| Инкай | Казахстан | 2007 |
| Доминион | ЮАР | 2007 |
| Рейнджер | Австралия | 1980 |
| Харасан | Казахстан | 2008 |
Запасы и объемы добычи урановой руды в России
Разведанные запасы урана в нашей стране оцениваются в более чем 400 тысяч тонн. При этом показатель прогнозируемых ресурсов составляет более 830 тысяч тонн. По состоянию на 2017 год в России действует 16 урановых месторождений. Причем 15 из них сосредоточены в Забайкалье. Главным месторождением урановой руды считается Стрельцовское рудное поле. В большинстве отечественных месторождениях добыча осуществляется шахтным способом.
Минералы, руды, добыча
В природе есть несколько урановых минералов:
- уранинит;
- настуран;
- карнотит;
- тюямунит.
Минералы можно отличить формами нахождения: в докембрийских, палеозойских, осадочных породах.
Основными месторождениями владеют Казахстан, Россия, Канада, Австралия.

Минералы урана
Добыча руды происходит тремя способами:
- Открытое. При залегании рудного тела близко к поверхности.
- Подземное. Руда глубоко под землей, пробиваются шахты, руду поднимают вверх на лифтах.
- Подземное выщелачивание. Бурят скважины, закачивают в них серную кислоту. Полученный раствор выкачивают и концентрируют.
Уран входит в состав ториевых и редкоземельных минералов.

Урановая руда
Свойства Урана

Уран (Uranium), 92-й элемент таблицы Менделеева, относится к металлам (семейство актиноидов).
Характеристики:
- структура решетки орторомбическая;
- имеет 3 кристаллические модификации;
- металл тяжелый, с высокой плотностью;
- слабый парамагнетик;
- металл радиоактивный.
Природный уран состоит из трех изотопов: 234U, 235U, 238U.
Радиоактивные свойства некоторых изотопов урана (жирным выделены природные изотопы):
Массовое числоПериод полураспадаОсновной тип распада2342,45⋅105 летα2357,13⋅108 летα2384,47⋅109 летα
| 233 | 1,59⋅105 лет | α |
| 236 | 2,39⋅107 лет | α |
| 237 | 6,75 сут. | β− |
| 239 | 23,54 минуты | β− |
| 240 | 14 часов | β− |
Стабильных изотопов нет.
Степень окисленияОксидГидроксидХарактерФормаПримечание
| +3 | Не существует | Не существует | — | U3+, UH3 | Сильный восстановитель |
| +4 | UO2 | Не существует | Основный | UO2, галогениды | |
| +5 | Не существует | Не существует | — | Галогениды | В воде диспропорционирует |
| +6 | UO3 | UO2(OH)2 | Амфотерный | UO22+ (уранил) UO42- (уранат) U2O72- (диуранат) | Устойчив на воздухе и в воде |
Химические свойства:
- Степени окисления от +3 до +6;
- Реагирует со многими неметаллами.
- С кислородом образует оксиды.
- Растворяется в кислотах: быстро — в HCl, HNO3, медленно в H2SO4, H3PO4, HF (формулы кислот).
- Не реагирует со щелочами.
Познавательно: радиоактивность металла изучали супруги Кюри-Склодовские более 100 лет назад. Их рабочие журналы до сих пор «фонят» так, что хранятся в свинцовых коробках.
Ученые говорят, что открыть их можно будет только через 1600 лет.
Свойства атомаНазвание, символ, номерАтомная масса(молярная масса)Электронная конфигурацияРадиус атомаХимические свойстваКовалентный радиусРадиус ионаЭлектроотрицательностьЭлектродный потенциалСтепени окисленияЭнергия ионизации(первый электрон)Термодинамические свойства простого веществаПлотность (при н. у.)Температура плавленияТемпература кипенияУд. теплота плавленияУд. теплота испаренияМолярная теплоёмкостьМолярный объёмКристаллическая решётка простого веществаСтруктура решёткиПараметры решёткиПрочие характеристикиТеплопроводностьНомер CAS
| Уран / Uranium (U), 92 |
| 238,02891(3)[1] а. е. м. (г/моль) |
| [Rn] 5f3 6d1 7s2 |
| 138 пм |
| 142 пм |
| (+6e) 80 (+4e) 97 пм |
| 1,38 (шкала Полинга) |
| U←U4+ -1,38В U←U3+ -1,66В U←U2+ -0,1В |
| 6, 5, 4, 3 |
| 686,4(7,11) кДж/моль (эВ) |
| 19,05 г/см³ |
| 1405,5 K |
| 4018 K |
| 12,6 кДж/моль |
| 417 кДж/моль |
| 27,67[2] Дж/(K·моль) |
| 12,5 см³/моль |
| орторомбическая |
| a = 2,854 Å; b = 5,870 Å; c = 4,955 Å[3] |
| (300 K) 27,5 Вт/(м·К) |
| 7440-61-1 |
Характеристики урана
- в обычных температурных условиях и под обычным давлением имеет твёрдую форму;
- имеет серебристо-серый цвет;
- является радиоактивным. Его радиоактивность возрастает при нагревании;
- имеет высокую плотность атомов.
Электронная схема урана
U: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f3 6d1
Короткая запись:
U: [Xe]6s2 4f14 5d10 6p6 7s2 5f3 6d1
Одинаковую электронную конфигурацию имеют атом урана и +2Pu, +3Am, +4Cm
Порядок заполнения оболочек атома урана (U) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на ‘d’ — до 10 и на ‘f’ до 14
Уран имеет 92 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
10 электронов на 5d-подуровне
6 электронов на 6p-подуровне
2 электрона на 7s-подуровне
3 электрона на 5f-подуровне
1 электрон на 6d-подуровне
Степень окисления урана
Атомы урана в соединениях имеют степени окисления 6, 5, 4, 3, 2.
Степень окисления — это условный заряд атома в соединении: связь в молекуле
между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается
заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается,
то степень окисления положительная.
Ионы урана
6+U
5+U
4+U
3+U
2+U
U 0
Валентность U
Атомы урана в соединениях проявляют валентность VI, V, IV, III, II.
Валентность урана характеризует способность атома U к образованию хмических связей.
Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании
химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа U
Квантовые числа определяются последним электроном в конфигурации,
для атома U эти числа имеют значение N = 6, L = 2, Ml = -2, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Самый тяжелый природный элемент
Тяжесть элемента может быть определена двумя способами; с точки зрения его атомного веса и с точки зрения его плотности. С 92 протонами в его ядре и атомным весом около 238,0289 уран является самым тяжелым природным элементом на Земле.
Самым тяжелым синтетическим элементом, известным на сегодняшний день, является Оганесон (атомный номер 118). С другой стороны, самым тяжелым элементом по плотности является осмий (22,59 г / см 3).
Изотопы урана
238U, 235U, 234U встречаются в природе в соотношении 99,3:0,7:0,0058, а 236U – в следовых количествах. Все другие изотопы урана от 226U до 242U получают искусственно. Изотоп 235U имеет особо важное значение. Под действием медленных (тепловых) нейтронов он делится с освобождением огромной энергии. Полное деление 235U приводит к выделению «теплового энергетического эквивалента» 2Ч107 кВтЧч/кг. Деление 235U можно использовать не только для получения больших количеств энергии, но также для синтеза других важных актиноидных элементов. Уран природного изотопного состава можно использовать в ядерных реакторах для производства нейтронов, образующихся при делении 235U, в то же время избыточные нейтроны, не востребуемые цепной реакцией, могут захватываться другим природным изотопом, что приводит к получению плутония:
При бомбардировке 238U быстрыми нейтронами протекают следующие реакции:
Согласно этой схеме, наиболее распространенный изотоп 238U может превращаться в плутоний-239, который, подобно 235U, также способен делиться под действием медленных нейтронов.
В настоящее время получено большое число искусственных изотопов урана. Среди них 233U особенно примечателен тем, что он также делится при взаимодействии с медленными нейтронами.
Некоторые другие искусственные изотопы урана часто применяются в качестве радиоактивных меток (индикаторов) в химических и физических исследованиях; это прежде всего b-излучатель 237U и a-излучатель 232U.
Самый нестабильный элемент
Все изотопы урана очень нестабильны, и это в основном из-за его размера. Том Зеллнер в своей книге «Уран: война, энергия и скала» описал уран примерно так: «Атом урана настолько перегружен, что он начал отливать из себя куски, как обманутый человек может сорвать с себя одежду».
Природный реактор ядерного деления
В 1972 году Фрэнсис Перрин обнаружил более десятка древних естественных ядерных реакторов, расположенных в трех отдельных рудных месторождениях на руднике Окло в Габоне (страна на западном побережье Центральной Африки). Эти реакторы деления неактивны. Последующие исследования показали, что им почти 2 миллиарда лет, за века до того, как был построен первый искусственный ядерный реактор.
Вам может быть интересно, как это возможно? Ну, чтобы понять это, вы должны сначала знать, что уран-235, который сегодня составляет всего около 0,72% природного урана, может выдерживать цепную реакцию деления, в отличие от урана-238. Он также разлагается гораздо быстрее, чем уран-238. Это означает, что уран-235 истощил намного больше, чем уран-238 с момента рождения Земли.
Если мы спроецируем это назад (2 миллиарда лет назад), то в урановой руде будет около 3% -3,6% урана-235, которого будет достаточно для поддержания цепной реакции ядерного деления. Таким образом, теоретически жизнеспособно существование древнего природного ядерного реактора.
Кристаллические формы
Характеристики урана обусловливают его реакцию с кислородом и азотом даже в нормальных условиях. При более высоких температурах он вступает в реакцию с широким спектром легирующих металлов, образуя интерметаллические соединения. Образование твердых растворов с другими металлами происходит редко из-за особых кристаллических структур, образованных атомами элемента. Между комнатной температурой и температурой плавления 1132 °C металлический уран существует в 3 кристаллических формах, известных как альфа (α), бета (β) и гамма (γ). Трансформация из α- в β-состояние происходит при 668 °C и от β до γ – при 775 °C. γ-уран имеет объемноцентрированную кубическую кристаллическую структуру, а β – тетрагональную. α-фаза состоит из слоев атомов в высокосимметричной орторомбической структуре. Эта анизотропная искаженная структура препятствует атомам легирующих металлов заменять атомы урана или занимать пространство между ними в кристаллической решетке. Обнаружено, что твердые растворы образуют только молибден и ниобий.
Соединения.
Уран – высокореакционноспособный металл – имеет степени окисления от +3 до +6, близок бериллию в ряду активности, взаимодействует со всеми неметаллами и образует интерметаллические соединения с Al, Be, Bi, Co, Cu, Fe, Hg, Mg, Ni, Pb, Sn и Zn. Тонкораздробленный уран особенно реакционноспособен и при температурах выше 500° С часто вступает в реакции, характерные для гидрида урана. Кусковой уран или стружка ярко сгорает при 700–1000° С, а пары урана горят уже при 150–250° С, с HF уран реагирует при 200–400° С, образуя UF4 и H2. Уран медленно растворяется в концентрированной HF или H2SO4 и 85%-ной H3PO4 даже при 90° С, но легко реагирует с конц. HCl и менее активно с HBr или HI. Наиболее активно и быстро протекают реакции урана с разбавленной и концентрированной HNO3 с образованием нитрата уранила (см. ниже). В присутствии HCl уран быстро растворяется в органических кислотах, образуя органические соли U4+. В зависимости от степени окисления уран образует несколько типов солей (наиболее важные среди них с U4+, одна из них UCl4 – легко окисляемая соль зеленого цвета); соли уранила (радикала UO22+) типа UO2(NO3)2 имеют желтую окраску и флуоресцируют зеленым цветом. Соли уранила образуются при растворении амфотерного оксида UO3 (желтая окраска) в кислой среде. В щелочной среде UO3 образует уранаты типа Na2UO4 или Na2U2O7. Последнее соединение («желтый уранил») применяют для изготовления фарфоровых глазурей и в производстве флуоресцентных стекол. КЕРАМИКА ПРОМЫШЛЕННАЯ.См. также
Галогениды урана широко изучались в 1940–1950, так как на их основе были разработаны методы разделения изотопов урана для атомной бомбы или ядерного реактора. Трифторид урана UF3 был получен восстановлением UF4 водородом, а тетрафторид урана UF4 получают разными способами по реакциям HF с оксидами типа UO3 или U3O8 или электролитическим восстановлением соединений уранила. Гексафторид урана UF6 получают фторированием U или UF4 элементным фтором либо действием кислорода на UF4. Гексафторид образует прозрачные кристаллы с высоким коэффициентом преломления при 64° С (1137 мм рт. ст.); соединение летуче (в условиях нормального давления возгоняется при 56,54° С). Оксогалогениды урана, например, оксофториды, имеют состав UO2F2 (фторид уранила), UOF2 (оксид-дифторид урана).
Уран в мире
Самые большие запасы урана находятся в Австралии. Затем идут Казахстан, Россия, Канада, ЮАР, Нигер и Бразилия.
Что касается производства электроэнергии с помощью атомных электростанций, то Канада, Казахстан и Австралия занимают лидирующие позиции. Эти три страны вместе производят более чем половину ядерной энергии в мире.
Смотрите таблицу с данными по производству и запасам урана каждой из перечисленных стран.
| Страна | Запасы урана (тысяч тонн / в год) | Производство обогащённого урана (тонн / в год) |
| Австралия | 1 661 | 7 743 |
| Казахстан | 629 | 7 994 |
| Россия | 487 | 3 239 |
| Канада | 468 | 10 485 |
| Нигер | 421 | 3 355 |
| Бразилия | 276 | 238 |
МАГАТЭ опубликовало полную, онлайновую, интерактивную и интегрированную цифровую карту распределения мировых запасов и месторождений урана. Это второе издание «World Distribution of Uranium Deposits» («Размещение урановых месторождений в мире») было подготовлено при участии Геологической службы провинции Саскачеван, Геологической службы Южной Австралии и Геологической службы Соединенных Штатов.
Информация в нем классифицирована по типам месторождений, и оно уникально в том смысле, что содержит огромный объем новой информации и знаний, сводя воедино данные из сотен открытых источников. Оно доступно каждому в режиме онлайн и включает в себя усовершенствованные интерактивные инструменты.
«Цель заключалась в том, чтобы составить сложную карту, которой очень просто пользоваться», — говорит Мартин Фэрклаф, специалист МАГАТЭ по урановому производству и один из составителей карты.
Эта карта была подготовлена для нужд управления ресурсами и запасами урана, геологических изысканий и содействия открытию и эксплуатации урановых месторождений. Она также содержит данные, имеющие отношение к реализации ядерно-энергетических программ по всему миру.
Карта основана на данных из базы данных МАГАТЭ «Размещение урановых месторождений в мире» (UDEPO), которые были уточнены в документах «Geological Classification of Uranium deposits and Description of Selected Examples» («Геологическая классификация урановых месторождений и описание отдельных примеров») и «IAEA UDEPO 2016 edition» («UDEPO МАГАТЭ, издание 2016 года»). UDEPO постоянно обновляется и включает в себя техническую информацию и подробные геологические данные о регионах, районах и месторождениях. Оба документа, служащие дополнением к карте, могут быть загружены онлайн.
Уран и ядерные бомбы
Для производства электроэнергии уран обогащают для того, чтобы содержание изотопа 235U составило 3 или 4 %.
Для производства же атомной бомбы его содержание должно быть 90 %.
Когда уран обогащён до таких показателей, ядерное деление путём нейтронной бомбардировки представляет собой серьёзный процесс. При аварии на ядерном реакторе последствия будут катастрофическими.
Бомба, сброшенная США на Хиросиму (город в Японии) в конце Второй мировой войны, называлась «Малыш» (от англ. Little boy). Она содержала 64 кг обогащённого урана. Разрушительная сила этой бомбы была равна 15 000 тоннам тротилового эквивалента.

Облако над Хиросимой после взрыва атомной бомбы
«Малыш» произвёл тепловую волну, температура которой достигла 4000 градусов, а её скорость равнялась 440 метрам в секунду.
Взрыв стал причиной гибели 80 000 человек. Тысячи людей подверглись радиации.
Помимо того, что атомная бомба прервала жизни многих людей, последствия радиации будут испытывать на себе бессчётное количество поколений жертв бомбардировки.
Получение
Основной задачей является производство продукта для ядерных реакторов. Это могут быть чистый металл, UO2, UF4.
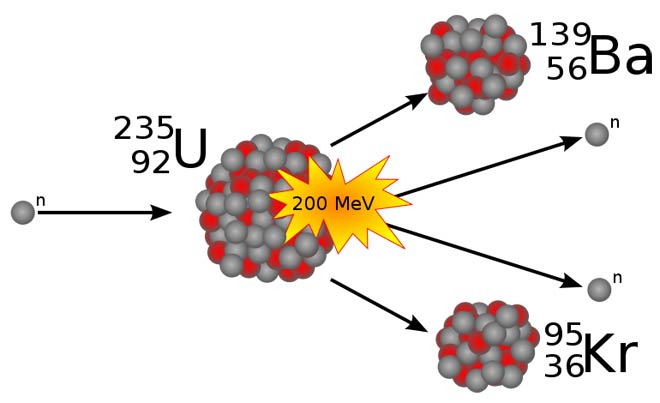
Схема деления 235U
Способ получения чистого урана:
- Концентрирование.
- Выщелачивание концентрата (перевод металла в раствор).
- Выделение урана методом экстракции или ионообменными смолами.
- Перевод продукта в оксид или тетрафторид.
- При надобности соединения переводят в UO2, UF4.
- Восстанавливают металлический уран.
Сплавы, соединения
В урановых сплавах применяют в качестве лигатуры:
- алюминий;
- титан;
- ванидий;
- ниобий;
- тантал и другие металлы.
Основными соединениями урана считают сплавы U-Al, U-Mg и U-Мо.
К сведению: оружейный уран легко превратить в топливный — просто «разбавить» обедненным (естественным).
Применение урана
После того, как урановую руду извлекают из земли, её измельчают, перерабатывают и делают небольшие урановые таблетки. Таблетки урана подвергаются высоким температурам, чтобы они стали более прочными.
Таблетки помещают в трубки, как правило, циркониевые. Каждая трубка вмещает до 335 таблеток. 236 трубок образуют топливную сборку или ТВЭЛ (тепловыделяющий элемент), которую затем помещают в ядерный реактор.
После того как топливо закладывается в реактор, начинается процесс ядерного деления. Деление происходит в результате бомбардировки нейтронами атомного ядра урана.
Когда нейтрон сталкивается с атомом урана, последний расщепляется на два других атома. Происходит выделение большого количества энергии и других нейтронов. Они сталкиваются с атомами и порождают цепную реакцию.
Выделяемая энергия становится теплотой, которая нагревает воду в реакторе. Пар от горячей воды активирует турбины, а те, в свою очередь, запускают электрогенераторы. Такие генераторы и производят электроэнергию.
Ядерная (атомная) энергетика России
В России функционируют 10 атомных электростанций.
Основные залежи урана в России находятся рядом с городом Краснокаменском. Там же находятся основные горно-химическое объединения и крупнейшее уранодобывающее предприятие.
По объёму добытого урана Россия занимает 5 место. А вот по запасам урана — 3 место.
Недостатки ядерной энергии
Одним из основных недостатков является риск аварий и их последствия для окружающей среды. Зоны, заражённые радиоактивностью урана, становятся непригодными для жилья.
Ядерные отходы — ещё одно негативное последствие. Остатки производства не могут быть использованы повторно и должны быть правильно утилизированы. Контакт людей с такими отходами может вызвать генетическую мутацию, болезни и даже немедленную смерть.

Бочки с ядерными отходами
Уран и производство электричества
Символ урана в периодической таблице — U. Уран состоит в основном из двух изотопов — 235U и 238U. Уран на 99,7 % состоит из изотопа 238U и только оставшиеся 0,7 % — это изотоп 235U.
Именно изотоп 235U, который составляет столь малый процент урана, позволяет получить энергию посредством расщепления ядра атома. Для производства электричества концентрация изотопа 235U должна составлять 3–4 %. Поэтому химики обогащают уран.
Обогащение урана можно провести двумя способами: с помощью ультрацентрифугирования или газовой диффузии. Оба метода разделяют изотопы и в результате концентрация 235U повышается.
Ядерная энергия считается чистой, потому что она не выделяет парниковые газы и её отходы достаточно малы. Другим преимуществом этой энергии то, что её легко транспортировать и она не требует много места для хранения.
Обогащённый уран прессуют в таблетки размером 1х1 см. Энергоотдача такой таблетки очень высока: две таблетки способны обеспечить энергией семью из 4 человек на 1 месяц.
Таким образом, уран является отличной альтернативой нефти и углю: чтобы произвести столько же электроэнергии, сколько производит 1 килограмм урана, потребуется 10 тонн нефти и 20 тонн угля. Это помимо негативных эффектов, которые последние оказывают на окружающую среду. К тому же нефть и уголь требуют много места.
Плюсы и минусы
Достоинств у урана много — он и на войне солдат, и в мирной жизни поможет, и вылечит.
Недостатком можно считать изменение механических свойств ТВЭЛов при работе в реакторе. Поэтому здесь применяется не чистый металл, а его сплавы с цирконием, алюминием, молибденом.
- https://www.uznaychtotakoe.ru/uran/
- https://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/URAN.html
- https://www.syl.ru/article/350939/himicheskiy-element-uran-svoystva-harakteristika-formula-dobyicha-i-primenenie-urana
- https://promdevelop.ru/industry/uranovaya-ruda-svojstva-primenenie-dobycha/
- https://TheMineral.ru/metally/uran
- https://k-tree.ru/tools/chemistry/periodic.php?element=U
- https://new-science.ru/15-intrigujushhih-faktov-ob-urane-slabyj-radioaktivnyj-metall/
- https://www.atomic-energy.ru/photo/92704





