Самые древние изделия из меди были найдены на территории современной Турции. Находились они в руинах поселения Чатал-Хююк. За каменным веком наступил медный век.
Содержание
- 1 История открытия
- 2 Общие данные
- 3 Химические свойства меди
- 4 Физические свойства меди
- 5 С чем реагирует
- 6 Кристаллическая решётка меди
- 7 Оптические свойства
- 8 Кристаллографические свойства
- 9 Температура плавления меди
- 10 Расчет удельного веса
- 11 Запасы, добыча
- 12 Медь в природе
- 13 Способы получения
- 14 Области применения меди
- 15 Медь в строительстве — токоотводы, кровля
- 16 Изделия из меди в повседневной жизни
- 17 Гидроксид меди применение
- 18 Оксид меди применение
- 19 Использование меди в медицине
- 20 5 Целебные свойства меди
- 21 18 интересных фактов о меди
История открытия
Ученые в XX веке смогли доказать, что с помощью инструментов, изготовленных из меди, можно быстрее обрабатывать материалы.
Из меди изготавливались сплавы с оловом, которые называются бронзой. Их применяли для создания украшений, инструментов, оружия. Когда бронза получила большую популярность, наступил бронзовый век, который сменил медный.
Первые большие рудники были найдена на территории Кипра. Они разрабатывались около 3000 лет до н. э. В России самые старые рудники датируются 2000 лет до н. э.
Промышленная выплавка медных слитков была освоена в XIII–XIV веке. В Москве в XV веке основался Пушечный двор, который производил орудия, боеприпасы из бронзы.
Общие данные
Расположение в периодической таблице Д.И. Менделеева: в старой версии — IV период, V ряд, I группа, в новой версии таблицы – 11 группа, 4 период.
- Атомный номер – 29
- Атомная масса – 63,546 г/моль
- Электронная конфигурация – [Ar] 3d10 4s1
- Температура плавления (°С) – 1083,4 (1356,55 K)
- Температура кипения (°С) – 2567.
- CAS: 7440-50-8.
Химические свойства меди
| 300 | Химические свойства | |
| 301 | Степени окисления | -2, 0, +1, +2 , +3, +4 |
| 302 | Валентность | I, II |
| 303 | Электроотрицательность | 1,90 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 745,48 кДж/моль (7,726380(4) эВ) |
| 305 | Электродный потенциал | Cu+ + e— → Cu, Eo = +0,520 В, Cu2+ + e— → Cu+, Eo = +0,153 В, Cu2+ + 2e— → Cu, Eo = +0,337 В |
| 306 | Энергия сродства атома к электрону | 118,4 кДж/моль |
Физические свойства меди
| 400 | Физические свойства | |
| 401 | Плотность* | 8,96 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело), 8,02 г/см3 (при температуре плавления 1084,62 °C и иных стандартных условиях, состояние вещества – жидкость), 7,962 г/см3 (при 1127 °C и иных стандартных условиях, состояние вещества – жидкость), 7,225 г/см3 (при 2027 °C и иных стандартных условиях, состояние вещества – жидкость), |
| 402 | Температура плавления* | 1084,62 °C (1357,77 K, 1984,32 °F) |
| 403 | Температура кипения* | 2562 °C (2835 K, 4643 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 13,26 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 300,4 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | 0,384 Дж/г·K (при 20 °C) |
| 410 | Молярная теплоёмкость | 24,44 Дж/(K·моль) |
| 411 | Молярный объём | 7,1 см³/моль |
| 412 | Теплопроводность | 401 Вт/(м·К) (при стандартных условиях), 401 Вт/(м·К) (при 300 K) |
| 413 | Коэффициент теплового расширения | 16,5 мкм/(М·К) (при 25 °С) |
| 414 | Коэффициент температуропроводности | |
| 415 | Критическая температура | |
| 416 | Критическое давление | |
| 417 | Критическая плотность | |
| 418 | Тройная точка | |
| 419 | Давление паров (мм.рт.ст.) | |
| 420 | Давление паров (Па) | |
| 421 | Стандартная энтальпия образования ΔH | |
| 422 | Стандартная энергия Гиббса образования ΔG | |
| 423 | Стандартная энтропия вещества S | |
| 424 | Стандартная мольная теплоемкость Cp | |
| 425 | Энтальпия диссоциации ΔHдисс | |
| 426 | Диэлектрическая проницаемость | |
| 427 | Магнитный тип | |
| 428 | Точка Кюри | |
| 429 | Объемная магнитная восприимчивость | |
| 430 | Удельная магнитная восприимчивость | |
| 431 | Молярная магнитная восприимчивость | |
| 432 | Электрический тип | |
| 433 | Электропроводность в твердой фазе | |
| 434 | Удельное электрическое сопротивление | |
| 435 | Сверхпроводимость при температуре | |
| 436 | Критическое магнитное поле разрушения сверхпроводимости | |
| 437 | Запрещенная зона | |
| 438 | Концентрация носителей заряда | |
| 439 | Твёрдость по Моосу | |
| 440 | Твёрдость по Бринеллю | |
| 441 | Твёрдость по Виккерсу | |
| 442 | Скорость звука | |
| 443 | Поверхностное натяжение | |
| 444 | Динамическая вязкость газов и жидкостей | |
| 445 | Взрывоопасные концентрации смеси газа с воздухом, % объёмных | |
| 446 | Взрывоопасные концентрации смеси газа с кислородом, % объёмных | |
| 446 | Предел прочности на растяжение | |
| 447 | Предел текучести | |
| 448 | Предел удлинения | |
| 449 | Модуль Юнга | |
| 450 | Модуль сдвига | |
| 451 | Объемный модуль упругости | |
| 452 | Коэффициент Пуассона | |
| 453 | Коэффициент преломления |
С чем реагирует
Медь НЕ реагирует с водородом, углеродом, азотом, а так же кремнием.
Реагирует с кислотами и солями, оксидами, галогенами, кислородом и неметаллами, но не может реагировать со щелочами, так как находится в электрохимическом ряду после водорода. Так же не может реагировать с фтором, бромом, хлором.
Отношение к кислороду
По отношению к кислороду металл проявляет слабую активность, но при длительном нахождении на воздухе покрывается очень тонкой, почти незаметной зеленоватой пленкой, которая и является оксидом меди.

В зависимости от температуры, при которой протекает реакция, купрум образует 2 оксида: CuO и Cu2O.
Взаимодействие с водой
По причине того, что медь находится в ряду электрохимического напряжения после водорода, она не вытесняет водород из воды. Но если присутствует кислород, водород может вытеснять молекулы металла, за счет чего и происходит окислительно-восстановительная реакция.
Реакции с кислотами
Из-за своего положения в электрохимическом ряду, не вытесняет водород из кислот, поэтому некоторые из них на нее не действуют. Но при достаточном доступе кислорода, растворяются в них, образуя соответствующие кислотам соли.
Отношение к галогенам и неметаллам
С галогенами медь реагирует довольно хорошо. В обычных условиях изменения не особо заметны, но на поверхности со временем образуется очень тонкий слой галогенидов. А при повышенных температурах реакция происходит очень быстро и бурно.

Cu реагирует с серой, в зависимости от температуры образуются следующие сульфиды: Сu2S, CuS.
Может образовывать йодиды (с йодом).
Реакции с оксидами неметаллов
Медь может реагировать не со всеми оксидами неметаллов, что зависит от неметалла, температуры и других условий протекания химической реакции.
С серой
Реакция серы с медью в зависимости от условий проведения может приводить к образованию как сульфида меди (I), так и сульфида меди (II). При нагревании смеси порошкообразных Cu и S до температуры 300-400оС образуется сульфид меди (I):
При избытке серы и проведении реакции при температуре более 400оС образуется сульфид меди (II). Однако, более простым способом получения сульфида меди (II) из простых веществ является взаимодействие меди с серой, растворенной в сероуглероде:
Данная реакция протекает при комнатной температуре.
С галогенами
С фтором, хлором и бромом медь реагирует, образуя галогениды с общей формулой CuHal2, где Hal – F, Cl или Br:
Cu + Br2 = CuBr2
В случае с йодом — самым слабым окислителем среди галогенов — образуется иодид меди (I):
С водородом, азотом, углеродом и кремнием медь не взаимодействует.
С кислотами-окислителями
- концентрированной серной кислотой
С концентрированной серной кислотой медь реагирует как при нагревании, так и при комнатной температуре. При нагревании реакция протекает в соответствии с уравнением:
Поскольку медь не является сильным восстановителем, сера восстанавливается в данной реакции только до степени окисления +4 (в SO2).
- с разбавленной азотной кислотой
Реакция меди с разбавленной HNO3 приводит к образованию нитрата меди (II) и монооксида азота:
3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 2NO↑ + 4H2O
- с концентрированной азотной кислотой
Концентрированная HNO3 легко реагирует с медью при обычных условиях. Отличие реакции меди с концентрированной азотной кислотой от взаимодействия с разбавленной азотной кислотой заключается в продукте восстановления азота. В случае концентрированной HNO3 азот восстанавливается в меньшей степени: вместо оксида азота (II) образуется оксид азота (IV), что связано с большей конкуренцией между молекулами азотной кислоты в концентрированной кислоте за электроны восстановителя (Cu):
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
С оксидами неметаллов
Медь реагирует с некоторыми оксидами неметаллов. Например, с такими оксидами, как NO2, NO, N2O медь окисляется до оксида меди (II), а азот восстанавливается до степени окисления 0, т.е. образуется простое вещество N2:
В случае диоксида серы, вместо простого вещества (серы) образуется сульфид меди(I). Связано это с тем, что медь с серой, в отличие от азота, реагирует:
С оксидами металлов
При спекании металлической меди с оксидом меди (II) при температуре 1000-2000 оС может быть получен оксид меди (I):
Также металлическая медь может восстановить при прокаливании оксид железа (III) до оксида железа (II):
С солями металлов
Медь вытесняет менее активные металлы (правее нее в ряду активности) из растворов их солей:
Cu + 2AgNO3 = Cu(NO3)2 + 2Ag↓
Также имеет место интересная реакция, в которой медь растворяется в соли более активного металла – железа в степени окисления +3. Однако противоречий нет, т.к. медь не вытесняет железо из его соли, а лишь восстанавливает его со степени окисления +3 до степени окисления +2:
Fe2(SO4)3 + Cu = CuSO4 + 2FeSO4
Cu + 2FeCl3 = CuCl2 + 2FeCl2
Последняя реакция используется при производстве микросхем на стадии травления медных плат.
Кристаллическая решётка меди
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Кубическая гранецентрированная
|
| 513 | Параметры решётки | 3,615 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 315 K |
| 516 | Название пространственной группы симметрии | Fm_ 3m |
| 517 | Номер пространственной группы симметрии | 225 |
Оптические свойства
| Цвет в отраженном свете | розовато-белый |
| Плеохроизм | не плеохроирует |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
Кристаллографические свойства
| Точечная группа | m3m (4/m 3 2/m) — гексоктаэдрический |
| Пространственная группа | Fm3m (F4/m 3 2/m) |
| Сингония | кубическая |
| Параметры ячейки | a = 3.615Å |
| Морфология | кубы, додекаэдры и тетрагексаэдры; редко октаэдры и сложные комбинации; нитевидные, древовидные |
| Двойникование | Двойники по {111} по шпинелевому закону |
Температура плавления меди
Плавится материал при определенной температуре, которая зависит от наличия и количества сплавов в составе.
В большинстве случаев, процесс происходит при температуре от 1085°. Наличие олова в сплаве дает разбег, плавление меди может начаться при 950°. Цинк в составе также понижает нижнюю границу до 900°.
Для точных расчетов времени понадобится график плавления меди. На обычном листке бумаги используется график, где по горизонтали отмечается время, а по вертикали градусы. График должен указывать, на каких моментах поддерживается температура при нагреве для полного процесса кристаллизации.

Печь для плавки меди
Расчет удельного веса
В настоящее время учеными разработано огромное количество способов, помогающих найти характеристики удельного веса меди, которые позволяют даже без обращения к специализированным таблицам вычислять этот немаловажный показатель. Зная его, можно с легкостью подобрать необходимые материалы, благодаря которым в конечном итоге можно получить нужную деталь с требуемыми параметрам. Это делается еще на стадии подготовки, когда планируется создать необходимую деталь из меди или ее содержащих сплавов.
Как уже говорилось выше, удельный вес меди можно подсмотреть в специализированном справочнике, но если под рукой такого нет, то его можно рассчитать по следующей формуле: вес делим на объем и получаем необходимую нам величину. Общими словами такое соотношение можно выразить как общее весовое значение к общему значению объема всего изделия.
Не стоит путать его с понятием плотности, так как он характеризует металл по-другому, хоть и имеет одинаковые значения показателей.
Рассмотрим, как можно вычислить удельный вес, если известна масса и объем медного изделия.
Например, имеем чистый медный лист толщиной 5 мм, шириной 2 м и длиной 1 м. Для начала посчитаем его объем: 5 мм * 1000 мм (1 м = 1000 мм) * 2000 мм, что составляет 10 000 000 мм3 или 10 000 см3. Для удобства расчетов будем считать, что масса листа составляет 89 кг 300 грамм или 89300 грамм. Делим рассчитанный результат на объем и получаем 8,93 г/см3. Зная этот показатель, мы всегда с легкостью можем вычислить весовое содержание в меди того или иного сплава. Это удобно, например, для обработки металла.
Единицы измерения удельного веса
В разных системах измерения используются разные единицы для обозначения удельного веса меди:
- В системе измерения СГС или сантиметр-грамм-секунда используется дин/см3.
- В Международной СИ используются единицы н/м3.
- В системе МКСС или метр-килограмм-секунда-свеча применяется кг/м3.
Первые два показателя равны между собой, а третий при конвертации равен 0,102 кг/м3.
Запасы, добыча
Глобальные объемы медной руды оцениваются в миллиард тонн (разведанные). Наличие половины подтверждено. Ученые полагают, что земная кора таит еще три миллиарда тонн меденосной руды.
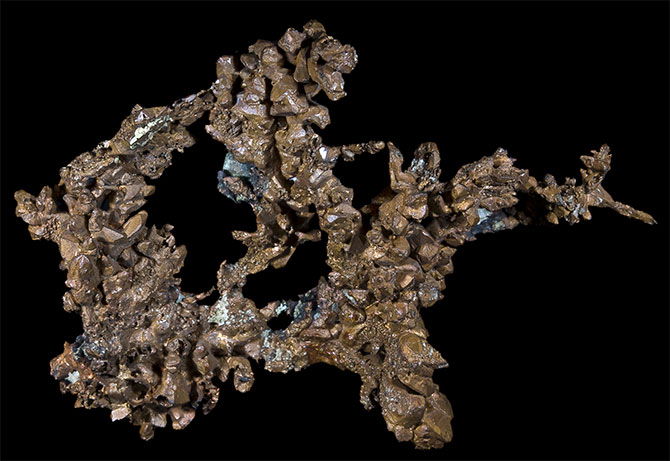
Самородная медь
Богатыми запасами располагают страны на всех континентах:
- Америка – Чили, Канада, США.
- Азия – Казахстан, Иран.
- Африка – ЮАР, Замбия, Заир.
На Россию приходится 3% мировых запасов. Месторождения сосредоточены на Урале. Основной добытчик – концерн «Норильский никель».
Руду добывают открытым либо закрытым способом, в зависимости от глубины залегания.
Ежегодный мировой объем добычи руды – 15-20 млн. тонн.
Медь в природе
В природе выявлено два проявления элемента – самородки и компонент соединений с другими элементами.

Самородок меди
Чаще это соединения: оксиды, сульфиды, гидрокарбонаты. Самое распространенное сырье – медный колчедан.
Медь придает глубокие синие, голубые, зеленоватые оттенки малахиту, бирюзе, хризоколле, другим минералам ювелирно-декоративного сегмента.
Способы получения
Содержание металла в рудах не превышает 2%. Поэтому перед плавкой их обогащают. Существует два способа получения меди: пиро- и гидрометаллургический.
Пирометаллургический
Многоуровневый процесс, включающий следующие этапы:
- Обогащение. Руды обогащают методом флотации. Взвешенные в воде медные частички «цепляются» к воздушным пузырькам, которые увлекают их на поверхность. На выходе получается порошок-концентрат с 12-36% меди.
- Обжиг. Процедура показана бедным (9-24% меди) медным рудам и концентратам, сильно «загрязненным» серой. При прокаливании с кислородом доля серы падает вдвое.
- Плавка. Кусками руды или порошком-концентратом загружают печи шахтного либо отражательного типа при 1452°С. Получают медный штейн.
- Продувка. В конвертерах на него воздействуют сжатым воздухом. Сульфиды и железо окисляются, образуется почти чистая (98,51 — 99,51%) черновая медь плюс железо, другие ценные компоненты в следовых количествах.
- Рафинирование. Черновой продукт отправляют на рафинирование – пламенем, затем электролитом. Примеси удаляются с газами. После первого этапа металл очищается до 99,51%, после заключительного – до 99,96%.
Способ применяется к 9/10 добытого сырья.
Гидрометаллургический
Состоит в обработке сырья растворенной серной кислотой малой концентрации и выделении металлического медного продукта.
Метод оптимален для руд с минимальным процентом меди. Извлечения других компонентов не предусматривается.
Области применения меди
Применение меди, как и наиболее схожего с ней по своим свойствам алюминия, хорошо известно — это производство кабельной продукции. Медные провода и кабели, характеризуются невысоким электрическим сопротивлением и особыми магнитными свойствами. Для производства кабельной продукции применяются виды меди, характеризующиеся высокой чистотой. Если в ее состав добавить даже незначительное количество посторонних металлических примесей, к примеру, всего 0,02% алюминия, то электрическая проводимость исходного металла уменьшится на 8–10%.
Невысокий вес меди и ее высокая прочность, а также способность поддаваться различным видам механической обработки — это те свойства, которые позволяют производить из нее трубы, успешно использующиеся для транспортировки газа, горячей и холодной воды, пара. Совершенно не случайно именно подобные трубы применяются в составе инженерных коммуникаций жилых и административных зданий в большинстве европейских стран.
Медь, кроме исключительно высокой электропроводности, отличается способностью хорошо проводить тепло. Благодаря этому свойству она успешно используется в составе следующих систем:
- тепловые трубки;
- кулеры, использующиеся для охлаждения элементов персональных компьютеров;
- системы отопления и охлаждения воздуха;
- системы, обеспечивающие перераспределение тепла в различных устройствах (теплообменники).
Металлические конструкции, в которых использованы медные элементы, отличаются не только небольшим весом, но и исключительной декоративностью. Именно это послужило причиной их активного использования в архитектуре, а также для создания различных интерьерных элементов.

Шина электротехническая медная
Медь в строительстве — токоотводы, кровля
При строительстве домов медь неизменно используется в качестве громоотводов, молниезащиты. Для молниезащиты используется медная жила толщиной 8 мм из чистейшей меди, то есть для этого необходимо медная проволока марки ММ, так как благодаря чистоте меди этой марки обеспечивается эффективный отвод тока. Также в строительстве используется листовая медь в качестве кровли. Медь, и так обладающая хорошими антикоррозионными свойствами, благодаря образованию патины на поверхности листов или ленты из раскисленной меди служат больше 2 веков, в течении жизни не менее пяти поколений владельцев дома.
Изделия из меди в повседневной жизни
Это металл применяется не только для производства промышленных товаров, изделия из меди можно встретить и в повседневной жизни:
- посуда;
- предметы интерьера;
- кованые оградки;
- скульптуры;
- монеты.
Все эти предметы можно найти чуть ли не в каждом доме.
Важную роль в сельском хозяйстве выполняет почвенные удобрения, содержащие медный купорос – он стимулирует активный рост различных культур, защищает их от вредителей, раствором купороса обрабатывают деревья, кустарники, семена.

Предметы интерьера из меди
При строительстве домов медные листы используют в кровельных работах. Известно, что данный металл стойкий к различным атмосферным явлениям, под их воздействием образуется защитный слой – патина, который имеет зеленоватый оттенок. Патина предотвращает коррозию металла, и крыша с таким покрытием может служить долгое время.

Медные монеты
К области применения меди можно отнести и гальванопластику, она известна еще с 1873 года. Гальванопластика представляет собой особый вид искусства, который базируется на электролитическом осаждении металла в водном растворе солей. Этот метод давно вышел за пределы искусства и применяется в космической отрасли, авиации, машиностроении. Суть его заключается в том, что созданный макет изделия, например, из гипса или пластилина, металлизируют, после удаления макета остается только металлическая форма. Процесс металлизирования происходит путем нанесения на макет тонкого слоя металла, чаще используют графит, помещают заготовку в раствор, который содержит соли меди. Макет играет роль катода и притягивает частицы металла, которые в дальнейшем и образуют форму готового изделия.
Гидроксид меди применение
Гидроксид меди, также ка и сульфат является отличным фунгицидом. Он защищается растения от различных болезней, как грибковых, так и бактериальных.
Плюсы использования гидроксида меди:
- широкий перечень инфекций, на которые действует соединение
- можно использовать практически для всех видов растений
- питательные вещества меди обеспечивают долгий срок хранения овощей и фруктов
- низкое содержание меди вследствие насыщения препаратов ионами Cu++
- устойчив к осадкам
- не оказывает негативного действия на природу
- невысокая стоимость.
Оксид меди применение
Оксид меди — CuO очень востребован в процессе изготовления стекла и эмалей. Он придает готовым изделиям зелёный и синий оттенок. Также оксид меди незаменим в производстве медно-рубинового стекла.
В лабораторных условиях он используется для выявления восстановительных качеств различных соединений. Вещество способно восстановить оксид до металлической меди. При этом наблюдается переход чёрного цвета оксида меди в розовый оттенок меди.
Использование меди в медицине
Традиционная медицина считает медь очень важным элементом жизнедеятельности человека. В организме это вещество содержится в количестве 2*10-4 % от общей массы. Ежедневно человек с пищей потребляет до 60 мг меди, из которых усваивается примерно 2 мг, что является необходимой нормой для здорового организма. Медь играет важную роль в биосинтезе гемоглобина, в поддержании уровня сахара, холестерина и мочевой кислоты. Для нормальной работы сердечно-сосудистой системы, головного мозга, пищеварительного тракта необходима медь. В случае ее недостатка развивается:
- анемия;
- остеопороз;
- глаукома;
- псориаз;
- бронхиальная астма;
- невриты;
- атрофия сердечной мышцы;
- утомляемость;
- потеря веса;
- накопление холестерина.
Применение меди в медицине:
- для лечения острой недостаточности используют лекарственные средства, содержащие этот микроэлемент;
- в терапии – использование металлических аппликаций или браслетов.
Наибольшее количество микроэлемента содержится в таких продуктах питания, как:
- шампиньоны;
- картофель;
- печень трески;
- цельное зерно;
- устрицы и каракатицы.
Вместе с тем избыток меди в организме, когда ее количество превышает 250 мг, ведет к интоксикации и нарушению работы печени, развитию болезни Вильсона, анемии.
5 Целебные свойства меди
Понятно, что плотность меди, ее вес и всевозможные химические и магнитные показатели, по большому счету, мало интересуют обычного человека. А вот целебные свойства меди хотят узнать многие.
Древние индийцы применяли медь для лечения органов зрения и различных недугов кожных покровов. Древние греки излечивали медными пластинками язвы, сильную отечность, синяки и ушибы, а также и более серьезные болезни (воспаления миндалин, врожденную и приобретенную глухоту). А на востоке медный красный порошок, растворенный в воде, применялся для восстановления сломанных костей ног и рук.
Лечебные свойства меди были хорошо известны и россиянам. Наши предки излечивали с помощью этого уникального металла холеру, эпилепсию, полиартриты и радикулиты. В настоящее время для лечения обычно используются медные пластинки, которые накладываются на специальные точки на теле человека. Целебные свойства меди при такой терапии проявляются в следующем:
- защитный потенциал организма человека возрастает;
- инфекционные болезни не страшны тем, кто лечится медью;
- наблюдается снижение болевых ощущений и снятие воспалительных явлений.
18 интересных фактов о меди
- Люди научились обрабатывать медь около 6 тысячелетий назад.
- Медь считается первым металлом, который древние люди стали массово применять в тех или иных областях.
- Знаете ли вы, что в природе медь в самородном виде встречается чаше, чем железо (см. интересные факты о железе)?
- Латинское название меди «Cuprum» произошло от названия острова Кипр, где этот металл добывали еще в 2 тысячелетии до н.э.
- Медный век продолжался в различных регионах приблизительно 1000-2000 лет. Он окончился после того, как человек освоил выплавку бронзы.
- Положением на сегодня, подавляющая часть электрических проводов производится именно из меди.
- Интересен факт, что в отличие от железа, медные предметы при столкновении друг с другом не способны вызывать искры.
- Из бронзы, в составе которой присутствует медь, делают дверные ручки и другие подобные изделия. Дело в том, что медь препятствует распространению бактерий, что является бесспорным преимуществом.
- Медь добавляют в разные сплавы, используемые для изготовления украшений.
- Любопытно, что медь является необходимым элементом для всех высших растений и животных.
- По объему мирового потребления медь находится на 3 месте после железа и алюминия (см. интересные факты об алюминии).
- Чилийский карьер Эскондида считается наибольшим на планете, где добывается медная руда.
- В организме взрослого человека содержится до 80 мг меди.
- Непальцы верят в то, что медь обладает целительными свойствами, вследствие чего пьют воду из сосудов, на дне которых находятся медные монеты.
- Благодаря высокой стойкости к коррозии из меди начали производить контейнеры для хранения токсичных и радиоактивных отходов.
- В Японии медным трубопроводам для газа проложенным в сооружениях присвоен статус «сейсмостойких».
- В древнеегипетских постройках ученые обнаружили медные водопроводные трубы, которым почти 5000 лет. Примечательно, что данные трубы по-прежнему находились в рабочем состоянии.
- Больше всего меди в организме человека сконцентрировано в печени.
Это были самые интересные факты о меди. Если вам понравилась эта статья, или вы вообще любите разные интересные факты, – поделитесь ею с друзьями 
- https://metalloy.ru/metally/med
- https://medicina.dobro-est.com/med-cu-rol-v-organizme-simptomyi-nedostatka-istochniki.html
- https://ChemicalStudy.ru/med-svoystva-atoma-himicheskie-i-fizicheskie-svoystva/
- https://Tarologiay.ru/nauka/himicheskie-i-fizicheskie-svoystva-medi.html
- https://scienceforyou.ru/teorija-dlja-podgotovki-k-egje/himicheskie-svojstva-perehodnyh-metallov
- https://mineralpro.ru/minerals/copper/
- https://stankiexpert.ru/spravochnik/materialovedenie/med.html
- https://jgems.ru/metally/med
- http://met-all.org/cvetmet-splavy/med/fizicheskie-i-himicheskie-svojstva-medi.html
- https://poliasmet.ru/svojstva-medi/primenenie-medi.html
- http://ecology-of.ru/med/oblast-primeneniya-medi/
- http://mining-prom.ru/cvetmet/med/96/
- https://tutmet.ru/med-lechebnye-himicheskie-svojstva-plotnost-jelektroprovodnost.html
- https://interesnyefakty.org/interesnye-fakty-o-medi/






