Звание первооткрывателя палладия принадлежит Вильяму Гайду Волластону.
Содержание
- 1 История открытия и названия
- 2 Характеристики и свойства
- 3 Классификация
- 4 Физические свойства
- 5 Оптические свойства палладия
- 6 Влияние на организм
- 7 Мистификация в мире платиноидов
- 8 Сравнение с другими металлами
- 9 Получение
- 10 Проба
- 11 Виды месторождений палладия
- 12 Добыча и использование
- 13 Где «водится» звездный металл
- 14 Промышленное применение металла
- 15 Ювелирное дело и инвестиции
- 16 Сколько стоит грамм палладия?
История открытия и названия
В 1803 году этому английскому химику удалось выделить новый элемент из южноамериканской платиновой руды. Опыт, в ходе которого Волластон получил палладий, состоял из нескольких этапов:
- Растворение руды в царской водке.
- Нейтрализация кислоты посредством раствора гидроксида натрия.
- Осаждение содержащейся в растворе платины при помощи хлорида аммония (он же нашатырь). Стоит отметить, что в осадок выпало не чистое вещество, а неорганическое соединение платины — гексахлорплатинат аммония.
- Добавление к раствору цианида ртути. В результате этих манипуляций получился цианид палладия — неорганическое соединение с формулой Pd (CN)2.
- Последний этап — выделение чистого вещества из полученного цианида в процессе нагревания.
Открытый элемент химик назвал в честь Паллады — астероида, обнаруженного одним немецким астрономом за год до открытия Волластона. Астероид же, в свою очередь, получил имя от древнегреческой богини Афины Паллады.
По легенде, изображение богини, названное палладиумом, упало с неба. Оказавшись в стенах Трои, этот талисман делал ее несокрушимой. Но после того как оберег палладиум был украден, великое царство пало.
Характеристики и свойства
В периодической таблице Менделеева палладий располагается под номером 46 в десятой группе (по вертикали) между никелем и платиной и в пятом периоде (по горизонтали) между родием и серебром. Принятое обозначение этого благородного металла — Pd, производное от латинского наименования Palladium.
Классификация
| Strunz (8-ое издание) | 1/A.14-20 |
| Nickel-Strunz (10-ое издание) | 1.AF.10 |
| Dana (7-ое издание) | 1.2.1.4 |
| Dana (8-ое издание) | 1.2.1.4 |
| Hey’s CIM Ref | 1.66 |
Физические свойства
| Цвет минерала | белый |
| Цвет черты | стальной серый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 4.5-5 |
| Прочность | ковкий |
| Излом | зазубренный |
| Плотность (измеренная) | 11.3 — 11.8 г/см3 |
| Радиоактивность (GRapi) | 0 |
| Магнетизм | парамагнетик |
Электронная схема палладия
Pd: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 4d10
Короткая запись:
Pd: [Kr]4d10
Порядок заполнения оболочек атома палладия (Pd) электронами:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d →
5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на
‘d’ — до 10 и на ‘f’ до 14
Палладий имеет 46 электронов, заполним электронные оболочки в описанном выше порядке:
Элемент Pd является исключением!
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
10 электронов на 4d-подуровне
Степень окисления палладия
Атомы палладия в соединениях имеют степени окисления 4, 2, 0.
Степень окисления — это условный заряд атома в соединении: связь в молекуле
между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается
заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается,
то степень окисления положительная.
Ионы палладия
4+Pd
2+Pd
Pd 0
Валентность Pd
Атомы палладия в соединениях проявляют валентность IV, II.
Валентность палладия характеризует способность атома Pd к образованию хмических связей.
Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании
химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Pd
Квантовые числа определяются последним электроном в конфигурации,
для атома Pd эти числа имеют значение N = 4, L = 2, Ml = -2, Ms = ½
Энергия ионизации
Чем ближе электрон к центру атома — тем больше энергии необходимо, что бы его оторвать.
Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo.
Если не указано иное, то энергия ионизации — это энергия отрыва первого электрона, также существуют энергии
ионизации для каждого последующего электрона.
Энергия ионизации Pd:
Eo = 804 кДж/моль
Оптические свойства палладия
| Тип | изотропный |
| Плеохроизм | не плеохроирует |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
Влияние на организм
Поскольку чистый палладий абсолютно безвреден для организма, из него изготавливают посуду, ювелирные украшения. Хлорид этого металла является очень ядовитым химическим веществом, которое при длительном контакте вызывает сильную интоксикацию организма.
Изотопы и воздействие на человека
Химия у многих людей вызывает негативные ассоциации, поэтому нелишним будет заострить внимание на том, обладает металл вредным воздействием на человека или является безопасным.
Натуральный, созданный природой элемент образуют шесть изотопов:
- 106Pd (27,34%);
- 108Pd (25,46%);
- 105Pd (22,34%);
- 110Pd (11,72%);
- 104Pd (11,14%);
- 102Pd (1%).
Изотопы стабильны, поэтому природный палладий безвреден. Но существует и разновидность, созданная искусственным путем. Это 107Pd — самый долгоживущий изотоп элемента. Он радиоактивен и, соответственно, опасен. Период его полураспада превышает семь миллионов лет.
Преимущественная часть изотопов имеет естественное природное происхождение. Но немало их формируется и в реакторах при процессе деления ядер плутония и урана. Образование палладия таким способом происходит постепенно. В современных ядерных установках размещается примерно 1,5 кг палладия на 1 тонну ядерного топлива (при условии 3%-ой степени выгорания).
Мистификация в мире платиноидов
История появления нашего героя в мире людей почти детективная.
В 1803 году Форстеру, солидному торговцу минералами, принесли сверток с письмом. В письме содержалась просьба продать три слитка металла, который (как уверяли в письме) ничем не уступает платине. Торговец знал толк в рекламе, воспользовался ими и в Лондоне разгорелись страсти. Ажиотаж умело подогревал Секретарь Королевского общества У. Г. Волластон.

Некий Ченевикс купил слиток и долго производил анализы; они показали, что это сплав платины и ртути. Другие химики и минералоги не нашли в слитках этих металлов.
Когда шумиха сошла на нет, в журнале «Nicholson’s Journal» было опубликовано объявление. Автор пообещал солидная сумму тому, кто за год синтезирует искусственный палладий. Интерес к слиткам снова возник, но приз остался неполученным.
А в 1804 году Волластон сообщил, что мистификация с новым металлом — его проделка. В это время он уже убедился, что палладий — это неизвестный дотоле элемент.

Уильям Волластон (1766—1828)
Процесс образования в природе
Основной источник появления — космические обломки метеоритов. В железных и каменных видах инопланетных осколков обнаружено большое содержание кристаллов драгметалла.
Структура, химические и физические свойства
По своей природе минерал выгодно отличается от прочих драгметаллов низким показателем плотности и химической инертностью. Благодаря последнему свойству он не взаимодействует с другими элементами и не окисляется.
Реакции:
- Исключениями являются кремний, бор, сера, хром, с ними палладий образует химические соединения.
- Также кристаллы металла растворяются в «царской водке» (это смесь двух кислот —серной и азотной).
По внешнему виду самородки аналогичны платине и серебру. Металл очень пластичный, благодаря чему активно используется в ювелирном деле. Для улучшения показателей прочности и износостойкости его берут в соединениях с другими металлами.
Температура плавления составляет 1554 градуса Цельсия.
Сравнение с другими металлами
Разницу между металлами часто ищут как в группах, получаемых из одной руды, так и в неродственных видах. Особенно часто это делается при выборе ювелирных изделий, когда нужно отличить палладий от серебра, белого золота или платины, определить, какой вариант сплава лучше. О том, что стоит учесть при сравнении палладия с другими металлами, лучше поговорить подробнее.
- Внешне палладий практически неотличим от серебра. При этом разница в цене у них существенная: 1 г палладия стоит как 100 г серебра. При этом со временем серебро темнеет, а палладий нет.
- С платиной основная разница состоит в удельном весе. Палладий легче, менее плотный (почти вдвое), растворяется в нагретой азотной кислоте. При проверке реагентом из царской водки и 10%-ной концентрации калия йодида у палладия будет реакция, а у платины нет.
- С золотом сравнение палладия сегодня происходит разве что в инвестиционной сфере. Здесь этот редкий металл уверенно опережает более широко известного конкурента. При наличии палладиевой лигатуры золото не теряет в цене.

Все эти факторы стоит учитывать при выборе металла для инвестиций. При покупке в слитках наиболее прибыльными по динамике цен сегодня считаются именно золото и палладий.
Получение
Элемент присутствует в белом золоте. И важная задача отделить его от висмута и мышьяка, которые, как и палладий, растворяются в азотной кислоте.
Чтобы это сделать, проделывают следующие манипуляции:
- Нитрат таких элементов, как серебро, палладий и висмут необходимо упарить до сиропного состояния. В случае с палладием это поможет удалить из них остатки различных кислот.
- Далее смесь разбавляется очищенной водой.
- Добавляется концентрированная соляная кислота. Образуется осадочный налет белого цвета, похожий на творог – хлорид серебра. Его необходимо отделить, чтобы раствор стал прозрачным.
- После этого состав упаривается. При этом происходит удаление соляной кислоты.
- В смесь добавляется аммиак. Состав должен стать синего или зеленого цвета. Начнут выпадать хлопья – хлорид висмута. Он не растворяется в аммиаке.
- Смесь фильтруется. К ней добавляется соляная кислота. В результате образуется сульфид палладия.
- После того как произойдет окончание реакции, образуется осадок желтого цвета в прозрачном растворе с желтоватым оттенком.
- Сульфид палладия необходимо тщательно промыть и избавить от воды.
- Далее сульфид палладия можно восстановить до состояния металла. Для этого его необходимо снова переплавить.
- Чтобы придать металлу товарный вид, сульфид палладия лучше всего восстанавливать с помощью сернистого водорода до черни. Затем его необходимо вновь сплавить. После этого сульфид палладия гранулируется.
Проба
Так как палладиум – металл мягкий, он не используется в чистом виде. Такой сплав не сможет выдержать даже небольшое внешнее воздействие.
Ювелиры используют для работы минерал с различными примесями. От их количества и названия зависит и проба сплава.
Основные пробы палладия представлены в таблице.
Проба Соединение
| 500 | В состав сплава входят 50% серебра или никеля. |
| 850 | Около 15% составляют серебро, никель или медь. |
| 950 | В состав входит около 5% рутения, меди или никеля. |
Все металлы придают элементу твердость. А если добавить золото или серебро, можно повысить износостойкость сплава.
Виды месторождений палладия
Сложнее всего Pd обнаружить в виде самородков. Гораздо чаще он входит в состав с другими минералами, после извлечения из недр отделяется путем химической обработки.
Месторождения делятся на 2 типа:
- Россыпные — представляют собой самородки, накапливавшиеся в течение долгих лет, расположены преимущество в районах рудных залежей.
- Коренные — представлены в большинстве, содержат соединения палладия с другими минералами.
Добыча и использование
Палладий – это драгоценный металлический сплав, который входит в состав более 30 минералов. Встречается и в виде самородков. Большое количество элемента входит в золотые и серебряные сплавы.

Палладіумъ считается редким драгоценным металлом. Он встречается гораздо реже, чем золото. Среди основных мест добычи можно выделить:
- Норильскую платину. Она является важным месторождением элемента. Здесь более половины от всех минералов составляет палладий. Остальная часть – ртуть, медь, никель.
- Большое количество металла добывается в Бразилии. Здесь находят самородки с содержанием элемента более 10%.
Применение металла палладиум различно. Нет практически ни одной области, где бы он не использовался:
- Благодаря своим удивительным свойствам металл широко применяется в химической промышленности. Элемент способен поглощать количество водорода в 1000 раз больше количества самого металла. Поэтому он используется как катализатор, например, при производстве маргарина. Это позволяет устранить возможность попадания в продукт никеля.
- Применяют этот элемент и для удаления водорода из растворов и газовых смесей. Сделать это можно, установив в качестве мембраны миллиметровую пластину из палладия.
- Сплавы из металла не поддаются окислению даже под электрической дугой. Это позволило применять минерал в электротехнической индустрии. Например, титан с незначительным добавлением палладия значительно увеличивает устойчивость состава к возникновению химических реакций.
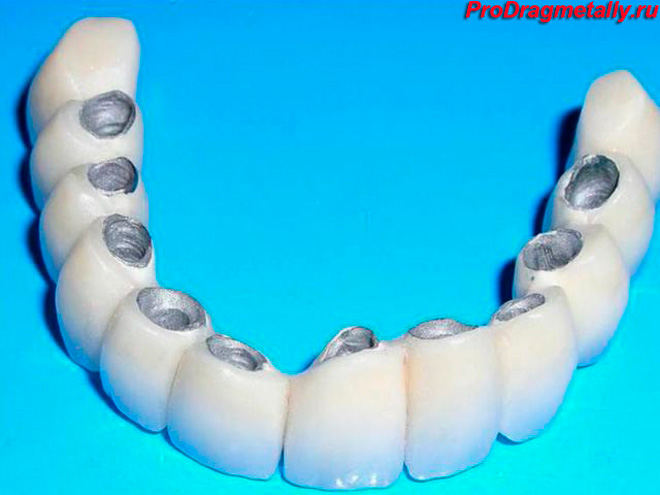
- Используется металл и в медицине, в частности, кардиологии, фармацевтике для производства ацетилена, в стоматологии для протезирования зубов. Элемент значительно снижает стоимость протезов, оставляя качество на высоком уровне.
- Применяют элемент и в промышленности – для производства труб. Металл может растягиваться до тех пор, пока нагрузка не составит 18,5 кг на 1 квадратный миллиметр. Добавляя родий с рутением, можно увеличить показатели сплава. Это позволяет создавать трубы без швов и спаек.
- Более 70% всей добычи минерала используется в машиностроении. Элемент применяется, как машинный катализатор, делая выхлопные газы более чистыми.
- Около 15% металла используется в электронной сфере производства.
- Всего 10% минерала применяется в ювелирном деле. Но данные сплавы высоко ценятся ювелирами. Наибольшую популярность имеет сплав с золотыми примесями, в результате чего получается золото, называемое белым. Благодаря своему мягкому блеску оно считается отличным окаймлением для бриллиантов.
Часто используется смесь палладия и платины. Она не только повышает технологические характеристики металла, но и придает украшению большую выразительность.
Способы добычи
Работа с палладиевыми месторождениями ведется в двух формах:
- закрытая (шахтная);
- открытая (карьерная).
В первом случае для добычи драгметалла создается система подземных туннелей — шахт. В найденном рудном пласте создаются небольшие по размерам отверстия, в которые затем закладывается взрывчатка. Разрыхленный взрывом грунт обрабатывается механизированным или ручным способом для извлечения частиц палладия. По окончании первичной очистки руда переправляется на поверхность, а затем транспортируется к месту дальнейшей переработки.
Для работы во втором случае привлекается тяжелая землеройная техника и транспорт для перевозки извлеченной руды. С ее помощью разрабатывают грунтовый карьер, из которого затем извлекают палладий. Далее ее перевозят для переработки на соответствующие предприятия.
Где «водится» звездный металл
Наш нынешний герой — редкость. Данные о запасах палладия разнятся: одни аналитики говорят, что его в 2-3 раза больше, чем золота, другие уверены, что минерал встречается в природе в 20 раз реже золота.
В природе часты образования палладия (твердого раствора) в самородной платине. Серебристый металл находят в виде зерен в россыпях платины.
Минералы палладийсодержащих руд:
- котульскит;
- майченерит;
- меренскиит;
- атокит;
- звягинцевит.
В России есть месторождения «брата платины» на Урале (Нижний Тагил); хребет Кондер в Хабаровском крае готов поделиться серебристым металлом; норильские месторождения Красноярского края — полное лукошко платиноидов.
Где встречается палладий в природе
В естественных условиях земных недр минерал содержится в виде соединений разных металлов. Подобные жилы встречаются и на территории Европы, и в РФ, и в Америке.
Мировые источники
Источники палладия в мире:
- ЮАР. Знаменитый Бушвельдский комплекс, здесь невообразимое количество минералов и руд. Платиноиды (почти 90% мирового запаса), хром, ванадий, железо, титан… Палладия тут производят 20% мировой добычи.
- Австралия, штат Новый Южный Уэльс. Добыча ведется из никелевых руд.
- Зимбабве. Тут, в Великой Дайке — огромном рудоносном районе хромитовых и платиновых минералов, находят палладиевые жилы.
- Бразилия, штат Минас-Жерайс. Россыпные месторождения.
- Канада, провинция Онтарио. Миллионы лет назад тут упал огромный метеорит, теперь люди собирают «подарки» — платиноиды, никель. Добычу ведут открытым способом.
- Колумбия, провинция Чоко. Россыпные платина, золото, палладий.
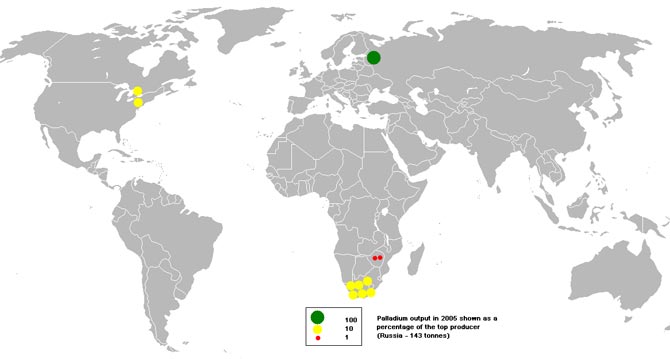
Основные районы добычи палладия
В России
Медно-никелевые месторождения, входящие в состав ОАО «ГМК «Норильский никель», являются крупнейшими в России поставщиками металла:
- Октябрьское;
- Талнахское;
- Норильск-1.
Их суммарная прибыль составляет более 40% от общемировой.

Промышленное применение металла
Добыча палладия на сегодняшний день удовлетворяет имеющийся на рынке спрос, который в основной своей части является промышленным. Применение Pd распределяется следующим образом:
- 70% — производство автомобильных катализаторов;
- 10% — электронная промышленность;
- 5% — химическая промышленность;
- 5% — медицина;
- 5% — инвестиции;
- 5% — ювелирное дело и другие сферы использования.
Основная часть добываемого металла используется для производства автомобильных катализаторов, именно поэтому спрос на Pd зависит от экономической ситуации в машиностроительной отрасли отдельно взятой страны-потребителя. Нейтрализаторы, содержащие палладий, необходимы при производстве автомобилей любых марок для дожигания выхлопных газов. Именно применение Pd вместо дефицитной в 2000-х годах платины привело к росту котировок этого драгметалла на мировых биржах. Дополнительным толчком стало решение ЕС об ограничении автомобильных выхлопов и ужесточении контроля за данной сферой. Катализаторы с содержанием Pd необходимы и для очистки газовых выбросов ТЭЦ.
Применение палладия в химической промышленности чрезвычайно широко. Являясь отличным катализатором, Pd незаменим при проведении процессов крекинга нефти и гидрогенизации жиров. Этот химический элемент в качестве катализатора используют при производстве ацетилена, аммиака, хлора, серной и азотной кислот, каустической соды, удобрений и фармацевтических средств. Хлорид палладия в промышленности применяют как индикатор для обнаружения микроколичеств угарного газа в газовых смесях.

Широко распространено использование металла в процессах глубокой очистки водорода, который активно диффундирует через палладий. Газ пропускают под давлением через нагретые палладиевые трубки, в итоге водород проходит через металл быстрее других примесей, которые задерживаются в трубках. Так как использование чистого палладия для этих целей является дорогостоящим, то в целях сокращения затрат на производство для очистки водорода применяют сплавы Pd с серебром или иттрием.
Pd и его сплавы используются в электронной промышленности. с его помощью создаются покрытия, отличающиеся устойчивостью по отношению к воздействию сульфидов. Металл нашел свое применение в производстве военной, аэрокосмической техники и аппаратуре гражданского назначения. Элемент необходим при выпуске реохордов, так как отличается высокой износоустойчивостью. Это свойства драгметалла отлично подходит для его использования в контактных группах. В гражданской аппаратуре Pd активно применялся в 80-х годах для контактов и струн советских контрольно-самопишущих машин и автоматических телефонных станций.

Так выглядит реохорд.
Где еще используется палладий? Он является компонентом керамических конденсаторов, известных всем радиолюбителям. Элемент присутствует в конденсаторах типа КМ, характеризующихся высокой температурной стабильностью емкости, которые присутствуют в любой высокочастотной радио- и телеаппаратуре, мобильных телефонах и компьютерах. Наличие Pd в радиодеталях привлекает любителей получения аффинажа металла в домашних условиях.
Металл нашел применение и в других сферах промышленного производства, где его используют для самых разных целей: палладий необходим для процесса изготовления специальной химической посуды, а также устойчивых к коррозии деталей измерительных приборов специального назначения. Pd незаменим и в стекольном деле, где его применяют в тиглях для варки стекла.
Палладий в последние годы все чаще используется в медицине. Металл и его сплавы расходуются на производство деталей различных медицинских приборов и инструментов. Самым простым примером применения Pd в этой отрасли является производство кардиостимуляторов, отдельные детали которых делаются именно из этого драгметалла. Иногда элемент используется для получения цитостатических препаратов.

В медицине наибольшая доля палладия тратится на изготовление зубных протезов. Развитие стоматологических исследований и увеличение сопутствующей потребности в металле способно увеличить спрос и котировки на элемент в будущем – этот фактор является одной из потенциальных причин роста стоимости Pd на биржах.
Применение в качестве катализаторов
Палладий прекрасный катализатор. В его присутствии начинаются и идут при низких температурах многие практически важные реакции, например, процессы гидрогенизации жиров и крекинга нефти. Процессы гидрирования многих органических продуктов палладий ускоряет гораздо лучше, чем другие испытанные катализаторы. Его используют в качестве катализатора при производстве ацетилена, многих фармацевтических препаратов, серной, азотной, уксусной кислот, удобрений, взрывчатых веществ, каустической соды, аммиака, хлора и других продуктов органического синтеза.
Хлорид палладия используется как катализатор и для обнаружения микро количеств угарного газа в воздухе или газовых смесях.
В аппаратуре химических производств катализатор из палладия, как правило, используют в виде «черни» (в тонкодисперсном состоянии палладий, как и все платиновые металлы, приобретает черный цвет) или в виде окисла PdO (в аппаратах гидрирования).
С семидесятых годов прошлого века палладий активно стала использовать автомобильная промышленность в катализаторах дожигания выхлопных газов (нейтрализаторы).
Применение в гальванотехнике
Хлорид палладия применяется в гальванотехнике, как активирующее вещество при гальванической металлизации диэлектриков — в частности, осаждении меди на поверхность слоистых пластиков при производстве печатных плат в электронике.
Очистка водорода
Если в сосуд, изготовленный из палладия, закачать под давлением водород, а затем нагреть закупоренную емкость, то водород «вытечет» из сосуда через стенки, как вода сквозь решето. При 240 °С за одну минуту через каждый квадратный сантиметр палладиевой пластинки толщиной в миллиметр проходит 40 кубических сантиметров водорода.
Это свойство палладия широко используется для очистки водорода. Под небольшим давлением газ пропускают через закрытые с одной стороны палладиевые трубки, нагретые до 600 °С. Водород быстро проходит через палладий, а примеси задерживаются в трубках. В результате получается особо чистый водород — с концентрацией 99,9999%. Для работы водородного топливного элемента нужен именно такой сверхчистый водород. Для удешевления процесса используют не чистый палладий, а сплавы его с другими металлами (серебро, иттрий).
Применение в медицине
Из палладия изготавливают некоторые медицинские инструменты. Благодаря своей высокой биологической совместимости он востребован при производстве электрокардиостимуляторов. Здесь особенно важно то, что палладий не вызывает аллергических реакций. Применяется этот благородный металл и в стоматологии: входит в состав сплавов, служащих материалом для зубных протезов. В последнее время его используют для производства противораковых препаратов.
Применение в электронной промышленности
Палладий и сплавы на его основе широко используются в электронике для покрытий, устойчивых к действию сульфидов. Этот металл идет на производство реохордов прецизионных сопротивлений высокой точности. В чистом виде палладий входит в состав керамических конденсаторов, с высокими показателями температурной стабильности ёмкости, которые нашли применение в производстве мобильных телефонов, компьютеров, широкоэкранных телевизоров и других электронных приборов.
Ювелирное дело и инвестиции
Ювелиры используют палладий как самостоятельный драгоценный металл, а также как компонент других драгоценных сплавов. Pd является компонентом лигатуры проб платины, а также практически всегда присутствует в качестве элемента золотых сплавов 585 и 750 пробы. Все известное и достаточно популярное на сегодняшний день белое золото обязано своим оттенком добавлению именно этого химического элемента. Сам драгметалл используется в производстве ювелирных украшений тоже не в чистом виде, в высоких пробах в лигатуре сплава присутствует рутений.
Для мировой добычи палладия спрос ювелирной отрасли не имеет решающего значения. Даже не смотря на политику популяризации палладиевых драгоценностей интерес потребителей к ним невелик. Ювелирные заводы предлагают своим клиентам как традиционные украшения для женщин – серьги, кольца, броши, подвески, так и мужские печатки, кресты и запонки. Драгметалл активно используется в последние годы в коллекциях известных модных дизайнеров, представляющих не только украшения, но и стильные и необычные аксессуары: часы, зажигалки, ручки, портмоне.
Где еще применяется драгоценный металл? Палладий по причине своего благородного происхождения относится к числу инвестиционных инструментов. Вложить средства в драгметалл можно разными способами, среди доступных вариантов для обычных клиентов банков числятся покупка слитков и открытие металлического счета. ОМС ведется в граммах «виртуального металла, поэтому при его открытии вы не получите ни грамма Pd на руки. А вот если вы решите приобрести слиток, то сможете ощутить вес металла в своих руках.

Палладий на рынке драгметаллов относят к числу фундаментальных активов, способных принести прибыль только в долгосрочном периоде. Большая часть инвестиций в металл представляет собой фьючерсные контракты на бирже, покупать палладиевые слитки с целью преумножения своих денег нет никакого смысла. Для начинающих инвесторов и обычных банковских клиентов проще всего будет открыть обезличенный счет. Другим своеобразным инвестиционным инструментов, непосредственно связанным с Pd, являются памятные монеты. Монеты из этого металла чеканятся редко и в ограниченном количестве, поэтому рассматривать их как источник получения прибыли нецелесообразно.
Ювелирные изделия из палладия
Палладиевые драгоценности можно встретить у многих отечественных и зарубежных брендов. Появление коллекции британского ювелира Стивена Веббера стало одним из самых значимых событий в мире моды. Веббер презентовал публике необычные серьги и броши из палладия, выполненные в старинном викторианском стиле.
Бренд Cartier тоже не побоялся экспериментировать и создал элегантные часы с палладиевым корпусом и россыпью бриллиантов в качестве декора. Немало интересных моделей можно найти в каталогах итальянской компании Antonini. Их общая черта – сочетание двух металлов. Золото символизирует традиции, а его платиновый собрат – современность.
Наиболее полно красоту украшений из палладия раскрыл ювелирный дом Tiffani & Co, в коллекциях которого представлены изысканные кольца, колье и серьги

Есть еще много компаний и частных мастеров, которые работают с этим материалом. Неудивительно, ведь палладий обладает подходящими физическими свойствами. Они наделяют готовые изделия такими преимуществами:
- износостойкость – поверхность не царапается и долго сохраняет первозданный внешний вид;
- оригинальность дизайна – чистый металл легко поддается обработке, он пластичный и мягкий. Для укрепления структуры его разбавляют серебром, никелем, рутением или медью;
- гипоаллергенность – материал не вызывает аллергических реакций. Но если в составе сплава присутствует никель, изготовленная из него вещь может представлять опасность для аллергиков;
- красивая наружность – палладиевые украшения имеют приятный жемчужный оттенок и блестящую поверхность с оптическим эффектом искрящейся фактуры.
Элемент относится к металлам платиновой группы, поэтому обладает всеми достоинствами платины. Он столь же прочен и устойчив к химическим и механическим повреждениям. Внешне материалы похожи и отличить их друг от друга непросто. Палладиевые изделия можно распознать по более светлому оттенку.

А как отличить палладий от серебра? Ведь и эти материалы похожи, на чем частенько пытаются заработать мошенники. Характерное отличие элемента Palladium – легкость.
При одинаковых размерах серебряное кольцо будет тяжелее платинового
В этом заключается еще одно преимущество украшений из современного металла – только они могут совмещать громоздкие габариты с небольшим весом.
Преимущества украшений из палладия
Для получения изделий из палладия используется сплав из основного металла и никеля, а также рутения и кобальта. На территории России возможно увидеть 950, 850 и 500 пробы металла. В ювелирных украшениях проба палладия играет важную роль — чем выше проба, тем податливее металл, мастера это знают и умело пользуются данной особенностью. Чаще всего встречаются украшения с пробой 500 и 850, а пробу 950 можно увидеть на обручальных кольцах, которые отличаются тем, что легче раскатываются для увеличения объема.
Химический элемент палладий относится к группе металлов платиновой группы и является очень легким драгметаллом. Это преимущество позволяет создавать легкие и объемные изделия. Особенность палладия заключается и в его низкой цене, по сравнению с белым золотом, серебром и платиной. В сравнении с серебром, украшения из палладия не тускнеют и не чернеют со временем.
Сколько стоит грамм палладия?
Раньше металл был одним из аутсайдеров благородной четверки и по цене превосходил лишь серебро. Но примерно пять лет назад образовался дефицит сырья в природе. С тех пор его стоимость растет как на дрожжах – к 2020 году она успела увеличиться на 180 %. Сегодня одна тройская унция палладия обходится покупателю в $2180. Он оценивается дороже основных конкурентов, у которых аналогичный показатель равен:

- золото – 1932 USD;
- платина – 912 USD;
- серебро – 27 USD.
В одной унции умещается 31 г. Соответственно, один грамм палладия стоит чуть больше семидесяти долларов
Стоимость готового изделия зависит от пробы. Чем меньше примесей в составе сплава, тем она выше. В Америке и Европе украшения делают из металла 950-й, 850-й и 500-й марки. Наши ювелиры работают только с двумя последними разновидностями, а самую дорогую обходят стороной. Между тем, именно палладий 950-й пробы считается самым красивым и наиболее подходящим для ювелирного дела.
На цену влияют и другие факторы: сложность дизайна, наличие драгоценных камней, именитость бренда. Сейчас эксклюзивные палладиевые украшения обходятся дороже золотых и платиновых. Но эксперты прогнозируют, что скоро сырье подешевеет и станет более доступным.
Сколько стоит 1 грамм. Актуальная цена на сегодня онлайн
Палладий | USD | 1 Унция
Цена за лом
При продаже Pd в качестве лома сложно заранее предугадать его стоимость. Металл чистейшей пробы в пунктах скупки может стоить на 20-30% дешевле рыночной цены в р./гр. При продаже украшений сплавов с вкраплениями других металлов скупщики смотрят не только на пробу, но и на суммарный вес изделий. Чем он больше, тем выше цена за 1 грамм.
Аналогичная ситуация и при продаже прочих товаров, содержащих палладий (спицы, радиодетали, монеты и т. д.). К тому же изредка стоимость определяется не по весу лома, а поштучно.
- https://VseoMetallah.ru/platina_gruppa/himicheskij-element-palladij
- https://mineralpro.ru/minerals/palladium/
- https://k-tree.ru/tools/chemistry/periodic.php?element=Pd
- https://metalloy.ru/metally/palladiy
- https://TheMineral.ru/metally/palladij
- https://zhazhdazolota.ru/drugie-dragmetally/chto-takoe-palladij
- https://vplate.ru/metally-i-splavy/o-palladii/
- https://ProDragmetally.ru/dragotsennye-metally/palladij/svojstva-i-tsena.html
- https://golden-inform.ru/prochee/palladij/
- https://mir-fin.ru/palladiy.html
- https://UvelirnoeDelo.ru/palladij-v-ukrasheniyah-preimushhestva-i-nedostatki-metalla/
- https://FB.ru/article/412689/ukrasheniya-iz-palladiya-proba-vidyi-ukrasheniy-osobennosti-izgotovleniya-i-foto-yuvelirnyih-izdeliy





